![]() Número 27, enero, 2026:
57–66
Número 27, enero, 2026:
57–66
ISSN versión impresa: 2071–9841 ISSN versión en línea: 2079–0139 https://doi.org/10.33800/nc.vi27.389
Nota científica
REGISTROS DEL TAMAÑO CORPORAL MÁXIMO DEL PEZ LEÓN,
PTEROIS VOLITANS (SCORPAENIDAE), ESPECIE INVASORA
REGISTRADA EN MÉXICO
Maximum body size records of the lionfish, Pterois volitans (Scorpaenidae), invasive species recorded in Mexico
Luis Fernando Del Moral-Flores1, Armando T. Wakida-Kusunoki2, Vicente Anislado-Tolentino3*y Jorge I. Rosales-Vásquez3a
1Laboratorio de Zoología, Facultad de
Estudios Superiores Iztacala, Universidad Nacional Autónoma de México,
Tlalnepantla, Estado de México, México. delmoralfer@gmail.com, ![]() https://orcid.org/0000-0002-7804-2716.
https://orcid.org/0000-0002-7804-2716.
2Centro Regional de Investigación
Acuícola y Pesquera de Yucalpetén. Instituto Mexicano de Investigación en Pesca
y Acuacultura Sustentables, México. armandowakida@yahoo.com.mx, ![]() https://orcid.org/0000-0002-79172651.
https://orcid.org/0000-0002-79172651.
3Grupo de Investigadores Libres Sphyrna,
Querétaro, México. acarcharodon.rosales@gmail.com, ![]() https://orcid.org/0000-0001-5245-3376.
https://orcid.org/0000-0001-5245-3376.
*Para
correspondencia: anislado@gmail.com, ![]() https://orcid.org/0000-0002-2184-0047.
https://orcid.org/0000-0002-2184-0047.
[Recibido: 01 de agosto, 2025; Aceptado: 19 de diciembre, 2025]
RESUMEN
El pez león Pterois volitans (Linnaeus, 1758) es una especie invasora que ha colonizado ampliamente el Atlántico occidental y sus poblaciones han incrementado en número y tamaño en comparación con las de sus áreas nativas. Se presenta el registro de talla corporal máximo reportado para las aguas mexicanas y del golfo de México, con base en un ejemplar de 430 mm de longitud total capturado en la plataforma continental de Alvarado, Veracruz. Se compara con los registros de talla para la especie reportados en México.
Palabras clave: especie no nativa, especie invasora, golfo de México, pez león colorado, Veracruz.
ABSTRACT
The lionfish Pterois volitans (Linnaeus, 1758) is an invasive species that has extensively colonized the Western Atlantic, its populations have increased in number and size compared to those in its native areas. The record of maximum body size reported for Mexican and Gulf of Mexico waters is presented, based on a specimen of 430 mm in total length captured on the continental shelf of Alvarado, Veracruz. It is compared with the size records for the species reported in Mexico.
Keywords: non-native specie, invasive species, Gulf of Mexico, red lionfish, Veracruz.
El pez león, Pterois volitans (Linnaeus, 1758), tiene una amplia distribución natural en el Pacífico occidental, desde el sur de Japón a la parte occidental de Australia, y se extiende hacia el oriente hasta las islas de Sumatra y Java (Kulbicki et al., 2012). Sin embargo, por malos manejos en el acuarismo se ha liberado de forma accidental en diversas regiones del mundo. En el Atlántico occidental, es una especie exótica e invasora con una rápida y amplia expansión, aumentando sus registros desde que se conocieron sus primeros reportes a mediados de la década de los ochenta (Schofield, 2009). A finales de la década de los noventa su presencia fue más frecuente en las costas de Florida (Schofield, 2010). La distribución actual de su invasión se ha expandido, abarcando actualmente desde Nueva York, EE. UU. (Meister et al., 2005) hasta el sureste de Brasil (Luiz et al., 2021).
La talla que presenta el pez león es importante a nivel ecológico, ya es un factor crucial que afecta a las especies nativas susceptibles a la depredación de esta especie (Benkwitt, 2013). Se conoce que los juveniles depredan principalmente crustáceos y conforme crecen, sus preferencias cambian hacia peces (Albins & Hixon, 2011; Morris & Akins, 2009). En el área de invasión se ha corroborado que los principales grupos taxonómicos que conforman su dieta son los peces, crustáceos y moluscos (Morris & Akins, 2009). Aguilar Medrano y Vega-Cendejas (2020) observan una dieta más diversa en el grupo 1 de talla-peso (valores medios = 17.74 cm y 112.4 g, respectivamente) en comparación con los de tallas y pesos mayores.
En algunas regiones del Caribe, las poblaciones del pez león han aumentado hasta alcanzar densidades intermedias en los sistemas arrecifales (Sabido-Itzá et al., 2016a). Este factor, junto con la presencia de grandes tallas en las áreas de invasión, en comparación con las tallas de las especies nativas, puede ocasionar problemas en la comunidad arrecifal (Darling et al., 2011; Pusack et al., 2016). La estructura de tallas y los grandes tamaños corporales que se han registrado en el Atlántico occidental (AO) (Aguilar-Perera et al., 2013; Ehemann, 2017) reflejan el alto crecimiento y adecuación poblacional en los nuevos ambientes de invasión (Côté & Maljković, 2010; Pusack et al., 2016). En Honduras se ha registrado la máxima talla del pez león en el AO con 480 mm de longitud total (Andradi-Brown et al., 2017). El objetivo de la presente contribución es registrar la máxima talla corporal del pez león en las costas mexicanas.
Durante un arrastre de pesca camaronera, el 22 de marzo de 2021, en la plataforma continental frente al municipio de Alvarado, Veracruz, a una profundidad cercana entre los 40 a 45 m (Fig.1), se capturaron dos organismos adultos de pez león. La especie corresponde a Pterois volitans (Linnaeus, 1758), y se determinó por medio de las características señaladas por Schultz (1986). Ambos ejemplares fueron fijados por formol (10%), preservados en alcohol etílico (70%) y depositados en la Colección Ictiológica de la Facultad de Estudios Superiores Iztacala, UNAM (CIFI-1451). Las medidas morfológicas fueron obtenidas con ayuda de un calibrador digital (0.1 mm).
El más grande de los ejemplares presentó 430 mm de longitud total (LT), 327 mm de longitud patrón (LP), 134 mm longitud prepectoral, 103 mm longitud predorsal, 129 mm longitud cefálica, 130 mm altura máxima; y su merística correspondiente fue de: aleta dorsal XII-I,11; anal III,7; pectoral 14; pélvica I,5; caudal 13 (Fig. 2). Desde su reporte en México, los registros y el monitoreo de la especie en los litorales mexicanos del golfo de México y el Caribe son más puntuales, incluyendo un aumento corporal de los ejemplares capturados (Tabla I).
Esta tendencia se ha visto reflejada en otros países del Caribe y el golfo de México.
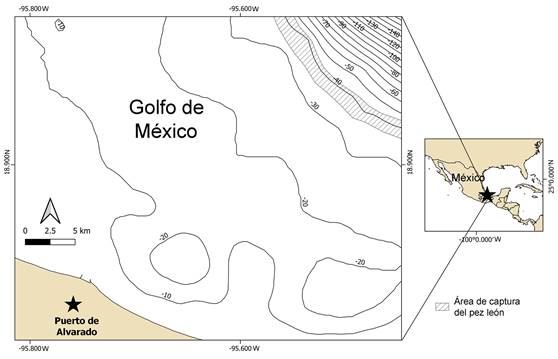
Figura 1. Mapa del área de captura del ejemplar del pez león, en la plataforma continental frente a Alvarado, Veracruz.

Figura 2. Vista lateral del pez león, Pterois volitans (CIFI-1451) capturado en la plataforma continental de Veracruz, México. Foto por Luis Fernando Del Moral-flores.
Tabla I. Longitudes corporales del pez León, Pterois volitans en mm, reportadas para México y otras áreas del Atlántico occidental con tallas superiores. LT = longitud total, LP = longitud patrón, SD = Sin datos.
|
MÉXICO Localidad (estado) |
LT |
LP |
Año |
Referencia |
|
Sistema Arrecifal Veracruzano (Veracruz) |
SD |
69-402 |
2018 |
Aguilar-Medrano & VegaCendejas (2020) |
|
Arrecife Alacranes (Yucatán) |
137 |
SD |
2009 |
Aguilar-Perera & Tuz-Sulub (2010) |
|
Costa norte, Arrecife Alacranes, Cayo Arenas (Yucatán) |
90-274 |
SD |
2010-2011 |
Aguilar-Perera et al. (2012) |
|
Cayo Arenas (Yucatán) |
390 |
SD |
2011 |
Aguilar-Perera et al. (2013) |
|
Arrecife Alacranes (Yucatán) |
98-358 |
SD |
2011-2013 |
Aguilar-Perera & QuijanoPuerto, (2016) |
|
La Pesca (Tamaulipas) |
151-162 |
129-137 |
2016 |
Arellano-Méndez et al. (2017) |
|
Isla Contoy-Xcalak (Quintana Roo) |
SD |
60-390 |
2011-2012 |
Arredondo-Chávez et al. (2016) |
|
Arrecifes de Cozumel (Quintana Roo) |
SD |
42-340 |
2013-2015 |
Bogdanoff et al. (2018) |
|
Sistema Arrecifal Veracruzano (Veracruz) |
90-397 |
SD |
2016-2017 |
Montoya-Mendoza et al. (2017) |
|
Arrecife Xcalak (Quintana Roo) |
70-380 |
SD |
2014-2015 |
Murillo-Pérez et al. (2021) |
|
Arrecife Alacranes (Yucatán) |
90-350 |
SD |
2010-2011 |
Perera-Chan & AguilarPerera (2014) |
|
Sistema Arrecifal Veracruzano (Veracruz) |
157-397 |
SD |
2016 |
Reyes-Aguilar et al. (2018) |
|
Sistema Arrecifal Veracruzano (Veracruz) |
185 |
SD |
2012 |
Santander-Monsalvo et al. (2012) |
|
Arrecifes de Xcalak (Quintana Roo) |
25-375 |
SD |
2009-2011 |
Sabido-Itzá et al. (2016a) |
|
Banco Chinchorro, Arrecife Xcalak (Quintana Roo) |
60-395 |
SD |
2012-2013 |
Sabido-Itzá et al. (2016b) |
|
Banco Chinchorro (Quintana Roo) |
50-400 |
SD |
2012-2013 |
Sabido-Itzá & García-Rivas (2019) |
|
San Pedro (Tabasco) |
245-250 |
SD |
2013-2014 |
Wakida-Kusunoki & Amador del Ángel (2015) |
|
Alvarado (Veracruz) |
430 |
327 |
2021 |
Presente estudio |
|
TALLAS MAYORES País (localidad) |
|
|
|
|
|
EE.UU. (Texas) |
75-444 |
SD |
2018 |
Blakeway et al. (2021) |
|
Venezuela (Isla Margarita) |
475 |
388 |
2015 |
Ehemann (2017) |
|
Honduras (Isla Útila) |
480 |
SD |
2014-2016 |
Andradi-Brown et al. (2017) |
Los registros de tallas más grandes de la especie corresponden al área de Carolina del Norte, EE. UU. (Muñoz et al., 2011), en Isla Margarita, Venezuela (Ehemann, 2017) e Isla de Útila en Honduras (Andradi-Brown et al., 2017), con 450, 457 y 480 mm de LT, respectivamente. Hay tallas reportadas de 476 y 490 mm LT en el Atlántico occidental, aunque se desconoce puntualmente los datos de las observaciones (Darling et al., 2011; Morris, 2012). En investigaciones sobre la alimentación de la especie en el Caribe mexicano y golfo de México, se han analizado especímenes con tallas que podrían estar cercanas a las máximas reportadas en la región (Aguilar-Medrano & Vega-Cendejas, 2020; Arredondo-Chávez et al., 2016). El aumento o registro de tallas más grandes, de acuerdo con Ehemann (2017), puede representar una tendencia ecológica importante.
En el golfo de México se ha estimado una edad de 4.5 años de un ejemplar de P. volitans de 385 mm de LT (Fogg et al., 2013). Aunque con recientes estudios con otolitos, se ha estimado el registro de mayor edad en noroeste del Golfo de México, con 10 años para un ejemplar de 375 mm de LT (Blakeway et al., 2021). Al utilizar la ecuación de edad y crecimiento estimada por Barbour et al. (2011), se puede inferir que el ejemplar de 430 mm reportado en este trabajo tendría una edad mayor a los ocho años, incluso el valor es superior a la edad máxima establecida en su modelo. De acuerdo con los estudios, la talla máxima reportada tiende a aumentar conforme la fase inicial de invasión se incrementa (Fogg et al., 2013; Switzer et al., 2015).
Se ha detectado una diferencia notable en las tasas de crecimiento, las poblaciones introducidas presentan un coeficiente de crecimiento que pueden doblar al de las nativas (Pusack et al., 2016). Esto puede estar correlacionado con una adaptación alimentaria y ventaja competitiva, al permitir consumir presas que tienen la mitad de su talla corporal, y al presentar una mayor talla son menos vulnerables a la depredación (Pusack et al., 2016). Sin embargo, es conocido que, a diferencia de las poblaciones nativas, en el Atlántico occidental no existen depredadores naturales u otras presiones que puedan regular el tamaño de los individuos o de las poblaciones (Côté et al. 2013). Además, la amplia gama de recursos alimenticios influye en favorecer la dinámica de la población invasora en comparación con las poblaciones nativas del Pacífico occidental. Si los mesodepredadores o competidores tuvieran poblaciones saludables en el Atlántico occidental, la competencia y depredación sobre el pez león podría apoyar a atenuar el impacto de la invasión del pez león. Las extracciones directas que han implementado diversos programas de control de pez león, pueden apoyar la regulación del crecimiento poblacional y de sus tamaños corporales. Se ha encontrado una disminución en la talla promedio del pez león en los arrecifes de coral de las Islas Caimán, después de una extracción continua que hicieron los buzos por más de siete meses (Frazer et al., 2012). A pesar de ser el método más efectivo, éste es viable solo en aguas someras (cercanas a las 35 m) y es necesario implementar otro tipo de técnicas a mayor profundidad (Switzer et al., 2015).
De acuerdo con Andradi-Brown et al. (2017), los organismos de P. volitans que se encuentran a mayor profundidad, como en los ecosistemas arrecifales mesofóticos (30 y 150 m), tienden a ser más grandes y hay una mayor proporción de hembras con desove activo, en comparación con los ejemplares capturados en arrecifes poco profundos. Esto coincide con lo reportado por ReyesAguilar et al. (2018), quienes reportan que los especímenes de mayores tallas del pez león en el Sistema arrecifal Veracruzano se encuentran en arrecifes más profundos o alejados de la línea de costa. Por lo tanto, esto podría explicar la captura del individuo motivo del presente estudio, ya que las profundidades donde los barcos camaroneros de la zona realizan principalmente sus actividades de pesca se encuentran entre 45 a 85 m (DOF, 2014) Muy probablemente la estrategia de segregación por tallas adoptada por el pez león minimiza la competencia interespecífica, aumenta la sobrevivencia al evitar a los posibles depredadores y la fecundidad, tal como se observa en algunos otros mesodepredadores (Jennings et al., 2001; Mindel et al., 2016).
Estas zonas profundas presentan mayores densidades del pez león y podrían estar sirviendo de refugio para evadir las actividades de erradicación (Andradi-Brown et al., 2017). Esta adecuación poblacional, podría, haber influido en la rápida propagación de la especie en el Atlántico occidental, ya que los peces de mayores tallas presentan una mayor fecundidad y viabilidad larval (Pusack et al., 2016). Por lo que es necesario registrar y monitorear puntualmente las tallas de los ejemplares en ambientes mesofóticos, así como buscar alternativas que incluyan la captura en aguas profundas para complementar los programas de erradicación que actualmente se llevan a cabo.
AGRADECIMIENTOS
Agradecemos a Juventino Arias, pescador local de Alvarado, Veracruz, quien obtuvo la muestra del pez león. Agradecemos al SNII-SECIHTI y al proyecto PAPIIT-IA27080 por el financiamiento otorgado. A L. F. Del Moral Magallón, por su apoyo en las distintas fases de campo. A los revisores y al editor principal, Gabriel de los Santos, por sus comentarios que enriquecieron y mejoraron la presente contribución.
REFERENCIAS
Aguilar-Medrano, R., & Vega-Cendejas, M. E. (2020). Size, weight, and diet on of the invasive lionfish Pterois volitans (Linnaeus, 1758) on the southern coast of Veracruz, Gulf of Mexico. Ciencias Marinas, 46(1), 57–64. https://doi.org/10.7773/cm.v46i1.3012
Aguilar-Perera, A., & Quijano-Puerto, L. (2016). Relations between fish length to weight, and otolith length and weight, of the lionfish Pterois volitans, in the Parque Nacional Arrecife Alacranes, southern Gulf of Mexico. Revista de Biología Marina y Oceanografía, 51(2), 469–474. https://doi.org/10.4067/S0718-19572016000200025
Aguilar-Perera, A., & Tuz-Sulub, A. (2010). Non-native, invasive red lionfish (Pterois volitans [Linnaeus, 1758]: Scorpaenidae), is first recorded in the southern Gulf of Mexico, off the northern Yucatan Peninsula, Mexico. Aquatic Invasions, 5, S9–S12. https://doi.org/10.3391/ai.2010.5.S1.003
Aguilar-Perera, A., Tuz-Sulub, A., Perera-Chan, L., López-Gómez, M. J., Triste, X. G., & Flota, E. C. (2012). Lionfish invasion off the northern coast of the Yucatan Peninsula, Mexico, Southern Gulf of Mexico: What do we know? Proceedings of the Gulf and Caribbean Fisheries Institute, 64, 34–38.
Aguilar-Perera, A., Perera-Chan, L., & Quijano-Puerto, L. (2013). Record body size for the red lionfish, Pterois volitans (Scorpaeniformes), in the Southern Gulf of Mexico. Gulf and
Caribbean Research, 25, 121–123. https://doi.org/10.18785/gcr.2501.10
Albins, M. A., & Hixon, M. A. (2011). Worst case scenario: potential long-term effects of invasive predatory lionfish (Pterois volitans) on Atlantic and Caribbean coral-reef communities. Environmental Biology of Fishes, 96, 1151–1157. https://doi.org/10.1007/s10641-011-9795-1
Andradi-Brown, D. A., Grey, R., Hendrix, A., Hitchner, D., Hunt, C. L., Gress, E., Madej, K., Parry, R. L., Régnier-McKellar, C., Jones, O. P., Arteaga, M., Izaguirre, A. P., Rogers, A. D., & Exton, D. A. (2017). Depth-dependent effects of culling-do mesophotic lionfish populations undermine current management? Royal Society Open Science, 4(5), 170027. https://doi.org/10.1098/rsos.170027
Arredondo-Chávez, A. T., Sánchez-Jiménez, J. A., Ávila-Morales, O. G., Torres-Chávez,
P., Herrerias-Diego, Y., Medina-Nava, M., Madrigal-Guridi, X., Campos-Mendoza, A., Domínguez-Domínguez, O., & Caballero-Vázquez, J. A. (2016). Spatio-temporal variation in the diet composition of red lionfish, Pterois volitans (Actinopterygii: Scorpaeniformes: Scorpaenidae), in the Mexican Caribbean: insights into the ecological effect of the alien invasion. Acta Ichthyologica et Piscatoria, 46(3), 185–200. https://doi.org/10.3750/AIP2016.46.3.03
Arellano-Méndez, L. U., Mora-Olivo, A., Zamora-Tovar, C., & Rosa-Manzano, E. (2017). First report of the invasive red lionfish Pterois volitans (Linnaeus, 1758) (Scorpaenidae) on the coast of Tamaulipas, Mexico. BioInvasions Records, 6, 255–258. https://doi.org/10.3391/bir.2017.6.3.11
Barbour, A. B., Allen, M. S., Frazer, T. K., & Sherman, K. D. (2011). Evaluating the potential efficacy of invasive lionfish (Pterois volitans) removals. PLoS One, 6(5), e19666. https://doi.org/10.1371/journal.pone.0019666
Benkwitt, C. E. (2013). Density-dependent growth in invasive lionfish (Pterois volitans). PLoS One, 8, e66995. https://doi.org/10.1371/journal.pone.0066995
Blakeway, R. D., Fogg, A. Q., & Jones, G. A. (2021). Oldest Indo-Pacific lionfish (Pterois volitans/P. miles) recorded from the Northwestern Gulf of Mexico. Gulf and Caribbean Research, 32(1), 1–4. https://doi.org/10.18785/gcr.3201.01
Bogdanoff, A. K., Mostowy, J., Peake, K., Layman, C. A., Brito-Bermudez, A., González Baca, C., Hernández-Palacios, N., Martinez-Gonzalez, D. T., Bravo-XiCoténcatl, M. R., & Morris, Jr. J. A. (2018). A brief description of invasive lionfish (Pterois sp.) diet composition in the Arrecifes de Cozumel National Park. Food Webs, 17, e00104. https://doi.org/10.1016/j.fooweb.2018.e00104
Côté, I. M. & Maljkovic´, A. (2010). Predation rates of Indo-Pacific lionfish on Bahamian coral reefs. Marine Ecology Progress Series, 404, 219–225. https://doi.org/10.3354/meps08458
Côté, I. M., Green, S. J., & Hixon, M. A. (2013). Predatory fish invaders: Insights from IndoPacific lionfish in the western Atlantic and Caribbean. Biological Conservation, 164,
50–61. https://doi.org/10.1016/j.biocon.2013.04.014
Darling, E. S., Green, S. J., O’Leary, J. K., & Côté, I. M. (2011). Indo–Pacific lionfish are larger and more abundant on invaded reefs: A comparison of Kenyan and Bahamian lionfish populations. Biological Invasions, 13, 2045–2051. https://doi.org/10.1007/s10530-011-0020-0
DOF, Diario Oficial de la Federación (2014). Acuerdo por el que se da a conocer el Plan de Manejo Pesquero de Camarón Café (Farfantepenaeus aztecus) y Camarón Blanco (Litopenaeus setiferus) en las costas de Tamaulipas y Veracruz. 12 marzo 2014 [En línea] https://www. gob.mx/cms/uploads/attachment/file/481591/PMP_Camaron_cafe_tamps_ver.pdf. (24 Dec 2022).
Ehemann, N. R. (2017). A new western Atlantic size record for Pterois volitans (Actinopterygii: Scorpaeniformes: Scorpaenidae) with new morphological data on head spinules. Acta Ichthyological et Piscatoria, 47, 297–301. https://doi.org/10.3750/AIEP/02149
Fogg, A. Q., Hoffmayer, E. R., Driggers, W. B. III, Campbell, M. D., Pellegrin, G. J., & Stein, W. (2013). Distribution and length frequency of invasive lionfish (Pterois sp.) in the norther Gulf of Mexico. Gulf and Caribbean Research, 25, 111–115. https://doi.org/10.18785/gcr.2501.08
Frazer, T. K., Jacoby, C. A., Edwards, M. A., Barry, S. C., & Manfrino, C. M. (2012). Coping with the lionfish invasion: can targeted removals yield beneficial effects? Reviews in Fisheries Science, 20, 185–191. https://doi.org/10.1080/10641262.2012.700655
Jennings, S., Pinnegar, J. K., Polunin, N. V. C., & Boon, T. W. (2001). Weak crossspecies relationships between body size and trophic level belie powerful size-based trophic structuring in fish communities. Journal of Animal Ecology, 70, 934–944. https://doi.org/10.1046/j.0021-8790.2001.00552.x
Kulbicki, M., Beets, J., Chabanet, P., Cure, K., Darling, E., Floeter, S. R., Galzin, R., Green, A., Harmelin-Viven, M., Hixon, M., Letourneur, Y., Lison de Loma, T., McClanahan, T., McIlwain, J., MouTham, G., Myers, R., O’LearY, J. K., Planes, S., Vigliola, L., & Wantiez, L. (2012). Distributions of Indo-Pacific lionfishes Pterois spp. in their native ranges: implications for the Atlantic invasion. Marine Ecology Progress Series, 446, 189–205. https://doi.org/10.3354/meps09442
Luiz, O. J., dos Santos, W. C. R., Marceniuk, A. P., Rocha, L. A., Floeter, S. R., Buck, C. E., de Klautau, A. G. C. M., & Ferreira, C. E. L. (2021). Multiple lionfish (Pterois spp.) new occurrences along the Brazilian coast confirm the invasion pathway into the Southwestern
Atlantic. Biological Invasions, 23, 3013–3019. https://doi.org/10.1007/s10530-021-02575-8
Meister, H. S., Wyanski, D. M., Loefer, J. K., Ross, S. W., Quattrini, A. M., & Sulak, K. J. (2005). Further evidence for the invasion and establishment of Pterois volitans (Teleostei: Scorpaenidae) along the Atlantic Coast of the United States. Southeastern Naturalist, 4, 193–206. https://doi.org/10.1656/1528-7092(2005)004[0193:FEFTIA]2.0.CO;2
Mindel, B. L., Neat, F. C., Trueman, C. N., Webb, T. J., & Blanchard, J. L. (2016). Functional, size and taxonomic diversity of fish along a depth gradient in the deep sea. PeerJ, 4, e2387. https://doi.org/10.7717/peerj.2387
Montoya-Mendoza, J., Camarena-Luhrs, T., Castañeda-Chávez, M. R., & Lango-Reynoso, F. (2017). Helminth parasites of red lionfish, Pterois volitans from the Veracruz Coral Reef System, Mexico, Southern Gulf of Mexico. Journal of Agricultural Science, 9, 30–33. https://doi.org/10.5539/jas.v9n11p30
Morris, Jr. J. A. (2012). Invasive lionfish: a guide to control and management. Gulf and Caribbean Fisheries Institute, Special Publication No. 1, 1–113.
Morris, J. A., & Akins, J. L. (2009). Feeding ecology of invasive lionfish (Pterois volitans) in the Bahamian archipelago. Environmental Biology of Fishes, 86, 389–398. https://doi.org/10.1007/s10641-009-9538-8
Muñoz, R. C., Currin, C. A., & Whitfield, P. E. (2011). Diet of invasive lionfish on hard bottom reefs of the Southeast USA: insights from stomach contents and stable isotopes. Marine Ecology Progress Series, 432, 181–193. https://doi.org/10.3354/meps09154
Murillo-Pérez, B. I., Schmitter-Soto, J. J., Cibián-Rojas, D., & Herrera-Pavón, R. L. (2021). Trophic overlap of lionfish (Pterois volitans) and two native predators (Lutjanus apodus and Cephalopholis cruentata) in the western Caribbean. Biota Neotropica, 21, e20190909. https://doi.org/10.1590/1676-0611-BN-2019-0909
Perera-Chan, L. C., & Aguilar-Perera, A. (2014). Length-weight and length-length relationships of the invasive red lionfish [Pterois volitans (Linnaeus, 1758): Scorpaenidae] in the Parque Nacional Arrecife Alacranes, Southern Gulf of Mexico. Journal Applicate Ichthyology, 30, 202–203. https://doi.org/10.1111/jai.12294
Pusack, T. J., Benkwitt, C. E., Cure, K., & Kindinger, T. L. (2016). Invasive red lionfish (Pterois volitans) grow faster in the Atlantic Ocean than in their native Pacific range. Environmental Biology of Fishes, 99, 571–579. https://doi.org/10.1007/s10641-016-0499-4
Reyes-Aguilar, A. R., Castañeda-Chávez, M. R., Montoya-Mendoza, J., Lango-Reynoso, F., Zamudio-Alemán, R. E., & Ramos-Miranda, J. (2018). Morphometry of Pterois volitans (Linnaeus, 1758) in the Veracruz Reef System in the Central Zone of the Gulf of Mexico. Oceanography & Fisheries, 5, 105–107. https://doi.org/10.19080/OFOAJ.2018.05.555673
Sabido-Itzá, M. M., Medina-Quej, A., de Jesús-Navarrete, A., Gómez-Poot, J. M., & GarcíaRivas, M. C. (2016a). La estructura de tallas como evidencia del establecimiento de Pterois volitans (Scorpaeniformes: Scorpaenidae) en el sur del Caribe mexicano. Revista de Biología Tropical, 64, 369–378.
Sabido-Itzá, M. M., Aguilar-Perera, A., & Medina-Quej, A. (2016b). Length-weight and length-length relations, and relative condition factor of red lionfish, Pterois volitans (Actinopterygii: Scorpaeniformes: Scorpaenidae), from two natural protected areas in the Mexican Caribbean. Acta Ichthyologica et Piscatoria, 46, 279–285. https://doi.org/10.3750/AIP2016.46.4.01
Sabido-Itzá, M. M., & García-Rivas, M. C. (2019). Record of abundance, spatial distribution and gregarious behavior of invasive lionfish Pterois spp. (Scorpaeniformes: Scorpaenidae) in coral reefs of Banco Chinchorro Biosphere Reserve, southeastern Mexico. Latin America Journal of Aquatic Research, 47, 349–355. https://doi.org/10.3856/vol47-issue2-fulltext-15 Santander-Monsalvo, J., López-Huerta, I., Aguilar-Perera, A., & Tuz-Sulub, A. (2012). First record of the red lionfish (Pterois volitans [Linnaeus, 1758]) off the coast of Veracruz, Mexico. BioInvasions Records, 1, 121–124. https://doi.org/10.3391/bir.2012.1.2.07
Schofield, P. J. (2009). Geographic extent and chronology of the invasion of non-native lionfish (Pterois volitans [Linnaeus 1758] and P. miles [Bennett 1828]) in the Western North Atlantic and Caribbean Sea. Aquatic Invasions, 4, 473–479. https://doi.org/10.3391/ai.2009.4.3.5
Schofield, P. J. (2010). Update on geographic spread of invasive lionfishes (Pterois volitans [Linnaeus, 1758] and P. miles [Bennett, 1828]) in the Western North Atlantic Ocean, Caribbean Sea and Gulf of Mexico. Aquatic Invasions, 5, 117–122. https://doi.org/10.3391/ai.2010.5.S1.024
Schultz, E. T. (1986). Pterois volitans and Pterois miles – 2 valid species. Copeia, 1986, 686– 690. https://doi.org/10.2307/1444950
Switzer, T. S., Tremain, D. M., Keenan, S. F., Stafford, C. J., Parks, S. L., & McMicheal, Jr R. H. (2015). Temporal and spatial dynamics of the Lionfish invasion in the Eastern Gulf of
Mexico: perspectives from a Boradscale Trawl Survey. Marine and Coastal Fisheries, 7, 1–8. https://doi.org/10.3354/meps10383
Wakida-Kusunoki, A. T., & Amador del Ángel, L. E. (2015). First record of the red lionfish, Pterois volitans, on the coast of Tabasco, México. Hidrobiológica, 25, 307–309.
Cómo citar: Del Moral-Flores, L. F., Wakida-Kusunoki, A. T., Anislado-Tolentino, & Rosales-Vásquez, J. I. (2026). Registros del tamaño corporal máximo del pez león, Pterois volitans (Scorpaenidae), especie invasora registrada en México. Novitates Caribaea, (27), 57–66. https://doi.org/10.33800/nc.vi27.389