![]() Número 27, enero, 2026:
1–17
Número 27, enero, 2026:
1–17
ISSN versión impresa: 2071–9841 ISSN versión en línea: 2079–0139 https://doi.org/10.33800/nc.vi27.386
GRUPOS MORFOECOLÓGICOS DE LA FAMILIA HISTERIDAE
(COLEOPTERA: POLYPHAGA) DE IMPORTANCIA CRIMINALÍSTICA EN CUBA
Morphoecological groups of criminalistic importance of the family Histeridae
(Coleoptera: Polyphaga) in Cuba
Yunier Lamoth-Mayet1 y Yoandri S. Megna2*
1Unidad
de Preparación y Ciencia, Dirección de Criminalística (DCrim), Calle Embil
esquina Sur, Altahabana, Boyeros, La Habana, Cuba. ylamothm@gmail.com, ![]() https://orcid.org/0009-0003-6845-8050.
https://orcid.org/0009-0003-6845-8050.
2Facultad de Ciencias Biológicas, Universidad Nacional Mayor de San Marcos, block 34, Av. Venezuela, Lima 15082, Perú.
*Para correspondencia:
ysmegna@gmail.com, ![]() https://orcid.org/0000-0002-5336-281X.
https://orcid.org/0000-0002-5336-281X.
[Recibido: 13 de marzo, 2025. Aceptado: 24 de septiembre, 2025]
RESUMEN
Las especies de la familia Histeridae son de interés criminalístico por su utilidad en la estimación del Intervalo Post Mortem (IPM). Sus adaptaciones morfológicas y ecológicas están relacionadas con su presencia en cadáveres en descomposición. Brasil, Argentina, Uruguay y Perú poseen listas de histéridos para estos estudios, en Cuba no se han definido cuáles pueden ser utilizadas con estos fines. El objetivo de esta investigación fue clasificar los histéridos de Cuba según su importancia criminalística, a partir de sus características morfoecología. Para ello, se realizaron colectas en trampas de caída con materia orgánica en descomposición, corteza de árboles podridos, en cadáveres de cerdos (Sus scrofa domestica), vacas (Bos taurus), caballos (Equus caballus) y humanos (Homo sapiens). También, se examinaron histéridos depositados en colecciones entomológicas cubanas. Se listan 50 especies de Histeridae para el archipiélago cubano, de estas 12 endémicas y el 41.1 % tienen importancia criminalística. Fueron reportadas especies de interés criminalístico sólo en el grupo de los geófilos, en el subgrupo de los saprófilos. Los resultados obtenidos constituyen el primer referente para un país de Centro América y el Caribe.
Palabras clave: Hydrophiloidea, postmortem, taxonomía, ecología, Antillas Mayores.
ABSTRACT
The species of the Histeridae family are forensic importance. due to their utility in estimating the Postmortem Interval (PMI). Their morphological and ecological adaptations are related to their presence in decomposing carcasses. While countries such as Brazil, Argentina, Uruguay, and Peru have established comprehensive lists of Histeridae species relevant to forensic investigations, no such compilation has yet been made for Cuba. The objective of this research was to classify the hister beetles from Cuba according to their forensic significance, based on their morphoecological characteristics. Samplings ware performed using fall traps with decomposing organic matter, in the bark of rotten trees, and carcasses of pigs (Sus scrofa domesticus), cows (Bos taurus), horses (Equus caballus), and humans (Homo sapiens). Also, Hister beetles from Cuban entomological collections were examined. A total of 50 Histeridae species were recorded from the Cuban archipelago, of which 12 are endemic and 41.1% have forensic significance. Three large morphoecological groups were identified: dendrophiles, geophiles, and microhistyrids. Species of forensic interest were reported only in the group of geophiles, in the subgroup of saprophiles. The results obtained constitute the first referent for a country in Central America and the Caribbean.
Keywords: Hydrophiloidea, postmortem, taxonomy, ecology, Greater Antilles.
INTRODUCCIÓN
La familia Histeridae está compuesta por alrededor de 4850 especies, distribuidas en 9 subfamilias (Lackner et al., 2024). Es un grupo de distribución mundial y ausente en las regiones polares. Pueden encontrarse en madrigueras de mamíferos, nidos de pájaros, colonias de hormigas y termitas, cuevas habitadas por murciélagos, nidos de abejas sin aguijón, zonas arenosas, hongos, madera y material vegetal en descomposición. Algunas son usadas como control biológico de especies de moscas y otras se encuentran en cadáveres en sus diferentes estados de descomposición (Kovarik & Caterino, 2000); esto les otorga relevancia en el ámbito criminalístico (Segura et al., 2009).
En Cuba, el estudio de los histéridos ha estado enfocado en general a resolver aspectos taxonómicos. Peck (2005) reportó 38 especies pertenecientes 16 géneros, 7 tribus y 6 subfamilias; en la presente actualización está compuesta por 50 especies pertenecientes a 19 géneros, 10 tribus y 6 subfamilias. En el presente siglo se ha comenzado a profundizar su utilidad por autores como Megna et al. (2021) y Naranjo et al. (2009). En este artículo se hace referencia al término criminalística y no forense en estudios sobre fauna cadavérica, por la influencia del Derecho Continental en las concepciones jurídicas de Cuba, criterio fundamentado por LamothMayet et al. (2025).
De acuerdo con Bala & Kaur (2014), Calzolari et al. (2014), Mise et al. (2013) y Santos et al. (2014) todas las especies de Histeridae son de importancia criminalística. Sin embargo, Yélamos (2002) plantea que en España no necesariamente todas las especies pueden colonizar cadáveres y propone una clasificación según sus hábitats. Esta aparente contradicción entre autores motiva la realización de la presente investigación.
OBJETIVOS
- Definir las especies de interés criminalístico de la familia Histeridae en Cuba.
MATERIALES Y MÉTODOS
Área de estudio
Cuba es un archipiélago compuesto por numerosas islas, una grande y estrecha (la más grande las de Antillas, con alrededor de 109 884 km2), la Isla de la Juventud (2419 km2) y un grupo de más de 4000 cayos e islotes (con un área total de alrededor de 3126 km2). Alrededor del 70 % de Cuba consiste en tierras llanas, con unas pocas sierras montañosas: en la región occidental la Sierra de Guaniguanico, en la región central Guamuahaya y en la región oriental la Sierra Maestra y Nipe–Sagua–Baracoa (Fig. 1).
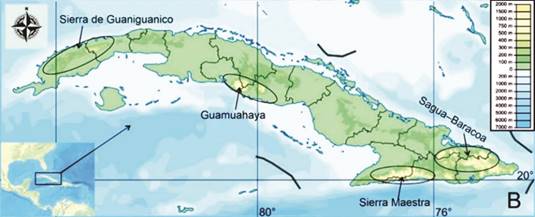
Figura 1. Áreas de estudio de la fauna de Histeridae en las Antillas.
Obtención de la información faunística, consulta bibliográfica y colecciones
Para obtener datos sobre la etología y ecología de los histéridos en Cuba se consultaron los trabajos de Sokolov (2005, 2016) y Yélamos (2002). Las informaciones sobre su actividad en cadáveres putrefactos, se obtuvo de las investigaciones sobre fauna cadavérica realizadas por Cobo & Lancis (1981), Lamoth-Mayet & Posada (2024), Megna et al. (2021) y Naranjo et al. (2009). Los ejemplares fueron recolectados por el método directo en trampas de caída con restos de pescado, en cadáveres de cerdos, vaca y humanos en descomposición (Anexo 1). Luego fueron conservados en alcohol al 96 % para su posterior identificación y depósito en las colecciones zoológicas.
Los ejemplares examinados fueron depositados en las siguientes colecciones:
CZCTR Museo de Historia Natural “Charles Ramsden”, Facultad de Ciencias Naturales, Universidad de Oriente, Santiago de Cuba, Cuba (M. Soto).
IZAC Instituto de Ecología y Sistemática (IES) de la Academia de Ciencias de Cuba.
Identificación y clasificación de grupos morfoecológicos de histéridos
Los ejemplares adultos fueron examinados mediante el uso de un estereoscópico NOVEL, modelo XSZ N-207. Se realizaron fotos de hábito en vista dorsal de las especies de interés criminalístico (Fig. 2). Para la clasificación de histéridos en Cuba, se asume la propuesta por Yélamos (2002), que establece los siguientes grupos: (1) los dendrófilos, que viven en troncos podridos; (2) los geófilos, que viven generalmente en hábitats relacionados con el suelo y se subdividen en saprófilos (se encuentran en materia orgánica en descomposición), psamófilos (en la base de plantas) y foleófilos (en nidos de aves y en madrigueras de mamíferos); por último, (3) los microhistéridos, que se encuentran en detritus vegetal, madera descompuesta y algas acumuladas en el litoral.

Figura 2. Vista dorsal de especies de interés criminalístico en Cuba. A) Phelister haemorrhous Marseul, 1854; B) Carcinops troglodytes (Paykull, 1811); C) Euspilotus arrogans (Marseul, 1855); D) Phelister panamensis LeConte, 1859; E) Xerosaprinus viator (Marseul, 1855); F) Atholus confinis (Erichson, 1834); G) Omalodes laevigatus (Quensel, 1806), H) Hister coenosus Erichson, 1834; I) Euspilotus cubaecola (Marseul, 1855).
RESULTADOS Y DISCUSIÓN
Contribución taxonómica a la familia Histeridae en Cuba
Los géneros de mayor número de especies son Aeletes Horn con 6, seguida de Carcinops Marseul con 5 y Euspilotus Lewis, Hololepta Paykull y Epierus Erichson con 4. Al culminar la investigación, para la familia Histeridae en Cuba se reportan 6 subfamilias, 10 tribus, 19 géneros y 50 especies, de ellas 12 endémicas (Tabla I). Los géneros Hypocaccus Thomson, Atholus Thomson, Iliotona Carnochan e Idolia Lewis presentan el menor número de especies con 1 (Tabla I). La mayor diversidad de la familia Histeridae en las Antillas aparece en Cuba con 50 especies, seguida por La Española (Haití y República Dominicana) con 20 (PerezGelabert, 2020). La mayor riqueza de histéridos en Cuba, se explica por la mayor superficie de este archipiélago en relación con las restantes islas, además de su gran diversidad de paisajes y ecosistemas (Genaro & Tejuca, 2001).
Grupos morfoecológicos de la familia Histeridae en Cuba
La familia Histeridae en Cuba pueden encontrarse bajo corteza de árboles caídos, excreta de vaca, en guano de murciélagos, arribazón de algas marinas, cadáveres humanos, de cerdos, vacas y caballos (Tabla III). Se clasifican en tres grupos morfoecológicos. Los dendrófilos, que están compuestos por especies de las subfamilias Histerinae (2 géneros y 5 especies) y Trypanaeinae (3 géneros y 6 especies). Los geófilos están subclasificados en saprófilos, compuestos por las subfamilias Histerinae (5 géneros y 10 especies), psamófilos, representado por Saprininae (1 género y 1 especie), foleófilos, representado por Dendrophilinae (1 género y 5 especies). El tercer grupo los microhistéridos, compuestos por las subfamilias Tribalinae (1 género y 4 especies) y Dendrophilinae (1 género y 2 especies) (Tabla II).
Las especies de interés criminalístico se encuentra en el grupo de geófilos, dentro del subgrupo de los saprófilos, encontrándose frecuentemente en cadáveres humanos en los estados enfisematoso y colicuativo (Tabla III). Estos histéridos pertenecen a las subfamilias Histerinae y Saprininae (Tabla III).
Las recolectas de histéridos con necrotrampas permitió confirmar que las especies del género Xerosaprinus Wenzel, suelen colonizar cadáveres en zonas costeras y montañosas (Tabla III). Estas también han sido identificadas en cadáveres de ganado mayor y humanos, en condiciones de sol y sombra para ambos períodos del año (lluvioso y poco lluvioso). Las del género Euspilotus Wenzel fueron observadas con mayor abundancia en zonas montañosas. A pesar de ser frecuentes en la materia orgánica de cerdos, vaca, caballo y humano, no se ha recolectado en excretas. De las especies del género registradas en Cuba, no se ha logrado recolectar Euspilotus sterquilinus (LeConte, 1860), que fue recolectada por Peck et al. (1998) sobre guano de murciélago en cuevas.
Por primera vez para un país de las Antillas se clasifican los histéridos según su morfoecología. En Cuba, están representados todos los grupos de histéridos propuestos por Yélamos (2002) en España.
Tabla I. Composición taxonómica de la familia Histeridae (*especies endémicas), († especies recolectadas en cadáveres en descomposición y necrotrampas).
|
Subfamilias (6) |
Tribus (10) |
Géneros (19) |
Especies (50) |
|
Abraeinae |
Acritini |
Acritus Le Conte |
1. Acritus analis LeConte, 1853 2. *Acritus atomus LeConte, 1862 3. Acritus ignobilis Lewis, 1888 |
|
Abraenini |
Aeletes Horn |
4. * Aeletes assimilis Wenzel, 1944 5. * Aeletes poeyi Marseul, 1862 6. * Aeletes rugiceps Wenzel, 1944 7. * Aeletes schwarzi Wenzel, 1944 8. Aeletes gulliver (Marseul, 1856) 9. Aeletes floridae Marseul, 1862 |
|
|
Saprininae |
Euspilotini |
Euspilotus Lewis |
10. †Euspilotus cubaecola (Marseul, 1855) 11. †Euspilotus arrogans (Marseul, 1855) 12. *Euspilotus sterquilinus (LeConte, 1860) 13. †Euspilotus campechianus (Erichson, 1834) |
|
Saprinus Erichson |
14. Saprinus cavallieri Marseul, 1855 15. Saprinus guayanensis Marseul, 1855 |
||
|
Xerosaprinus Wenzel |
16. *†Xerosaprinus fulgidus (LeConte, 1860) 17. †Xerosaprinus viator (Marseul, 1855) |
||
|
Hypocaccus Thomson |
18. Hypocaccus lustrans (Casey, 1916) |
||
|
Dendrophilinae |
Paromalini |
Carcinops Marseul |
19. Carcinops parvulus LeConte, 1860 20. Carcinops troglodytes (Paykull, 1811) 21. * Carcinops golovkoi Sokolov, 2003 22. Carcinops dominicanus Marseul 1855 23. Carcinops pumilio (Erichson, 1834) |
|
Paromalus Erichson |
24. Paromalus hispaniolae Marseul, 1870 25. Paromalus parallelus LeConte, 1860 26. Paromalus productus Marseul, 1855 |
||
|
Bacaniini |
Bacanius Le Conte |
27. Bacanius scalptus Lewis, 1888 28. Bacanius debilitans Casey, 1893 |
|
|
Trypanaeinae |
- |
Trypanaeus Eschscholtz |
29. Trypanaeus flavipennis Marseul, 1860 30. Trypanaeus luteivestis Marseul, 1860 |
|
Histerinae |
Hololeptini |
Hololepta Paykull |
31. Hololepta cubensis Erichson, 1834 32. Hololepta interrupta Marseul, 1853 33. Hololepta minuta Erichson, 1834 34. Hololepta quadridentatum (Oliver, 1789) |
|
Iliotona Carnochan |
35. *Iliotona markushevae Sokolov, 2003 |
||
|
Omalodini |
Omalodes Erichson |
36. †Omalodes laevigatus (Quensel, 1806) 37. Omalodes ruficlavis Marseul, 1853 |
|
|
Exosternini |
Baconia Lewis |
38. Baconia riehli (Marseul, 1862) 39. *Baconia pulchella Caterino, 2013 |
|
|
Phelister Marseul |
40. †Phelister haemorrhous Marseul, 1854 41. †Phelister completus Schmidt, 1893 42. †Phelister panamensis LeConte,1859 |
||
|
Histerini |
Atholus Thomson |
43. †Atholus confinis (Erichson, 1834) |
|
|
Hister Linnaeus |
44. †Hister coenosus Erichson, 1834 45. Hister servus Erichson, 1834 |
||
|
Tribalinae |
- |
Epierus Erichson |
46. Epierus antillarum (Marseul, 1854) 47. *Epierus cylindricus Wenzel, 1944 48. Epierus pulicarius (Erichson, 1834) 49. *Epierus smaragdinus Marseul, 1862 |
|
Idolia Lewis |
50. Idolia laevissima (J. L. LeConte, 1852) |
Tabla II. Composición taxonómica de los grupos morfoecológicos de la familia Histeridae en Cuba (** Grupo de interés criminalístico, *** Subfamilias de interés criminalístico).
|
Grupos (3) |
Subgrupos (4) |
Subfamilias |
Géneros |
Especies |
|
Dendrófilos |
|
Histerinae |
Hololepta |
1. Hololepta cubensis 2. Hololepta interrupta 3. Hololepta minuta 4. Hololepta quadridentatum |
|
Iliotona |
5. Iliotona markushevae |
|||
|
Trypanaeinae |
Trypanaeus |
6. Trypanaeus flavipennis 7. Trypanaeus luteivestis |
||
|
Idolia |
8. Idolia laevissima |
|||
|
Paromalus |
9. Paromalus hispaniolae 10. Paromalus parallelus 11. Paromalus productus |
|||
|
Geófilos** |
Saprófilo |
Histerinae*** |
Phelister |
12. Phelister completus 13. Phelister haemorrhous 14. Phelister panamensis |
|
Baconia |
15. Baconia pulchella 16. Baconia riehli |
|||
|
Hister |
17. Hister coenosus 18. Hister servus |
|||
|
Atholus |
19. Atholus confinis |
|||
|
Omalodes |
20. Omalodes laevigatus 21. Omalodes ruficlavis |
|||
|
Saprininae*** |
Saprinus |
22. Saprinus cavallieri 23. Saprinus guayanensis |
||
|
Xerosaprinus |
24. Xerosaprinus fulgidus 25. Xerosaprinus viator |
|||
|
Euspilotus |
26. Euspilotus arrogans 27. Euspilotus cubaecola 28. Euspilotus campechianus 29. Euspilotus sterquilinus |
|||
|
Psamófilos |
Saprininae |
Hypocaccus |
30. Hypocaccus lustrans |
|
|
Foleófilos |
Dendrophilinae |
Carcinops |
31. Carcinops dominicanus 32. Carcinops golovkoi 33. Carcinops parvulus 34. Carcinops pumilio 35. Carcinops troglodytes |
|
|
Mirmecófilos
|
Tribalinae |
Epierus |
36. Epierus antillarum 37. Epierus cylindricus 38. Epierus pulicarius 39. Epierus smaragdinus |
|
|
Dendrophilinae |
Bacanius |
40. Bacanius debilitans 41. Bacanius scalptus |
||
|
Microhistéridos |
|
Abraeinae |
Acritus |
42. Acritus analis 43. Acritus atomus 44. Aeletes assimilis |
|
Aeletes |
45. Aeletes floridae 46. Aeletes gulliver 47. Aeletes poeyi 48. Aeletes rugiceps 49. Aeletes schwarzi 50. Acritus ignobilis |
Tabla III. Sustratos de recolección y períodos tanatológicos más frecuentes de los grupos morfoecológicos de la familia Histeridae en Cuba (P: Período).
|
Grupos |
Subgrupos |
Especies |
Sustrato |
Períodos tanatológicos |
|
|
Dendrófilos |
|
1. Hololepta cubensis |
En corteza de árboles podridos (IZAC) |
|
|
|
|
|
2. Hololepta interrupta |
En corteza de árboles podridos (IZAC) |
|
|
|
|
|
3. Hololepta minuta |
En corteza de árboles podridos (IZAC) |
|
|
|
|
|
4. Hololepta quadridentatum |
En corteza de árboles podridos (IZAC) |
|
|
|
5. Iliotona markushevae |
Cactus podridos (Sokolov 2016) |
|
|||
|
6. Trypanaeus flavipennis 7. Trypanaeus luteivestis |
Bajo cortezas de árboles en el suelo (Gundlach, 1891) |
|
|||
|
8. Idolia laevissima |
Bajo corteza de árboles podridos (Sagra, 1857) |
|
|||
|
Geófilos |
Saprófilos |
9. Phelister completus |
Cadáveres de cerdos (Datos personales) |
Enfisematoso |
|
|
|
|
10. Phelister haemorrhous |
Excretas de vaca (Sokolov, 2005), caballo, cadáveres de cerdo y humano (Datos personales) |
Enfisematoso Colicuativo |
|
|
|
|
11. Phelister panamensis |
Excretas de vaca (Sokolov, 2005), caballo, cadáveres de cerdo (Datos personales) |
Enfisematoso |
|
|
12. Baconia pulchella 13. Baconia riehli |
|
|
|||
|
14. Hister coenosus |
Excretas de vaca, caballo, cadáveres de cerdo y humano, necrotrampas |
Enfisematoso Colicuativo |
|||
|
|
|
15. Hister servus |
En carnes corrompidas (Sagra, 1857) |
|
|
|
16. Atholus confinis |
Excretas de vaca, caballo, cadáveres de cerdo (Datos personales) |
Colicuativo |
|||
|
17. Omalodes laevigatus |
Necrotrampas (Datos personales) |
|
|||
|
|
|
18. Omalodes ruficlavis |
Cactus podrido (Sokolov, 2016) |
|
|
|
19. Saprinus cavallieri |
En excremento de rumiantes (Sagra, 1857) |
|
|||
|
|
|
20. Saprinus guayanensis |
Cadáveres de vaca (Datos personales) |
|
|
|
21. Xerosaprinus fulgidus |
Necrotrampas (Datos personales) |
|
|||
|
|
|
22. Xerosaprinus viator |
Necrotrampas, excretas de vaca (Sokolov, 2005), cadáver humano (Datos personales) |
Enfisematoso |
|
|
23. Euspilotus arrogans |
Necrotrampas y cadáver humano (Datos personales) |
Enfisematoso |
|
|
|
24. Euspilotus campechianus |
Cadáveres humanos (Datos personales) |
Colicuativo |
|
|
|
25. Euspilotus cubaecola |
Cadáveres de cerdo, humano y necrotrampas (Datos personales) |
Enfisematoso Colicuativo |
|
|
Cont. Tabla III
![]()
|
26. |
Euspilotus sterquilinus |
Sobre guano húmedo en cuevas (Peck et al., 1998) |
|
Psamófilos 27. |
Hypocaccus lustrans |
Entre algas muertas (Sokolov, 2005) |
|
Foleófilos 28. |
Carcinops dominicanus |
Bajo la corteza de árboles podridos (Sokolov, 2005) |
|
29. |
Carcinops golovkoi |
Cactus podrido (Sokolov, 2016) |
|
30. |
Carcinops pumilio |
|
|
31. |
Carcinops parvulus |
|
|
32. 33. |
Carcinops troglodytes |
Sobre guano húmedo en cuevas (Peck et al., 1998), sobre excretas de caballo (Datos personales) |
|
Paromalus hispaniolae |
|
|
|
34. |
Paromalus parallelus |
|
|
35. |
Paromalus productus |
Bajo corteza de árboles (Sagra 1857) |
|
Mirmecófilos 36. |
Epierus antillarum |
Bajo la corteza de árboles podridos (Datos personales), (Sokolov, 2005), Sobre guano húmedo en cuevas (Peck et al., 1998) |
|
37. |
Epierus cylindricus |
|
|
38. |
Epierus pulicarius |
|
|
39. 40. |
Epierus smaragdinus |
|
|
Bacanius debilitans |
|
|
|
41. |
Bacanius scalptus |
En el tronco de árboles podridos caídos (Mazur, 1972) |
|
Microhistéridos 42. |
Acritus analis |
Sobre guano húmedo en cuevas (Peck et al., 1998) |
|
43. Acritus atomus 44. Acritus ignobilis |
En corteza de árboles podridos (Sokolov, 2005) |
|
45. Aeletes assimilis
46. Aeletes floridae
47. Aeletes gulliver Cactus podridos (Sokolov, 2016)
48. Aeletes poeyi
49. Aeletes rugiceps
50. Aeletes schwarzi
![]()
A partir de los lugares de recolectas y del material examinado en colecciones, este estudio permitió definir que la mayoría de las especies de las subfamilias Histerinae (excepto las especies de los géneros Hololepta Paykull e Iliotona Carnochan) y de Saprininae en su totalidad constituyen especies de interés criminalístico en Cuba (Tablas II-III). El valor criminalístico de estas subfamilias también es abordado por Aballay et al. (2013). Estas especies según Yélamos (2002) corresponden al grupo de los Geófilos.
Se destaca que Carcinops troglodytes (Paykull, 1811) a pesar de pertenecer a la subfamilia Dendrophilinae, se ha recolectado en guano húmedo en cuevas por Peck et al. (1998) y sobre excretas de caballo, por lo que puede ser encontrada en cadáveres en descomposición, criterio confirmado por Aballay et al. (2013) los cuales la consideran una especie de interés forense.
Fueron identificadas en total 21 especies de importancia criminalística. En Cuba, se pueden encontrar con frecuencia especies de Histeridae en estiércol de vaca y caballo por caminos cubiertos de vegetación y pastizales aún en ausencia de cadáveres en descomposición. Otras en estado adulto son encontradas en estudios de sucesiones de insectos con cerdos en descomposición (BattánHorenstein et al., 2012) y en cadáveres humanos (Aballay et al., 2012; Mariani et al., 2014). Algunas especies han sido reportadas en hormigueros y cadáveres en descomposición, donde se desarrollan larvas de hormigas y dípteros, respectivamente (Arriagada et al., 2019).
Se conoce poco sobre la etología de las especies del género Omalodes Erichson. Sin embargo, O. laevigatus (Quensel, 1806) fue colectada en necrotrampas al sol y a la sombra, pero abundan más en zonas montañosas. Las del género Phelister Marseul fueron muy frecuentes en excretas de vaca, necrotrampas y cadáveres humanos (Megna et al., 2021). En ocasiones coinciden P. haemorrhous Marseul, 1854 y P. panamensis LeConte, 1859 en las excretas de vaca (Tabla III). Megna et al. (2021) han reportado P. completus Schmidt, 1893 sólo en cadáveres humanos al sol y a la sombra.
El género Hister Linnaeus está representado en Cuba por H. coenosus Erichson, 1834 e H. servus Erichson, 1834. Esta última, aún no ha sido recolectada en necrotrampas ni en cadáveres en descomposición (Tabla III). Hister coenosus Erichson, 1834 es muy común en necrotrampas, en excretas de vaca y cadáveres de ganado y humanos (Tabla III). Las especies del género Atholus Thomson, habitan en material vegetal en descomposición, animales muertos y estiércol (Lundyshev, 2017), lo cual coincide con nuestro estudio (Tabla III).
El hallazgo de Carcinops troglodytes (Paykull, 1811) en excretas de caballo guarda relación con lo reportado por Peck (2005) y Peck et al. (1998), quienes mencionan que esta especie utiliza las cuevas para completar su ciclo de vida, pero puede encontrarse fuera de estas. En el caso de los géneros Idolia Lewis, Paromalus Erichson y Baconia Lewis, se ubicaron a partir de la información de la literatura del grupo. Sagra (1857) reporta haber recolectado a Idolia laevissima (J. L. LeConte, 1852) en corteza de árboles podridos. Yélamos (2002) refiere que las especies del género Paromalus por su cuerpo cilíndrico, pueden encontrarse desplazándose en las galerías de troncos de árboles y corteza podridas alimentándose de pequeñas larvas, huevos y exuvias de insectos, ácaros y hongos.
De igual forma, el género Baconia Lewis pertenece a la tribu Exosternini, en la región Neotropical, las especies de esta tribu representan aproximadamente un tercio de la diversidad de especies conocidas de la familia Histeridae y exhiben notables extremos de variedad morfológica. Estas especies se asocian a vegetación en descomposición, estiércol y carroña, otras son mirmecófilas y termitófilas (Caterino & Tishechkin, 2015). Este criterio anterior, incluye a las especies de Baconia Lewis dentro de las especies de interés criminalístico.
La presencia de histéridos en los estados enfisematoso y colicuativo, confirma lo planteado por Castillo-Miralbés (2002) quien las clasifica como especies necrófilas por alimentarse de larvas de dípteros a partir del tercero y cuarto día de iniciada la descomposición. En este período se incrementa su actividad a medida que aumenta el desarrollo de larvas de dípteros y disminuye su actividad al iniciar la etapa esquelética.
AGRADECIMIENTOS
Este trabajo fue subvencionado por el CONCYTEC a través del programa PROCIENCIA en el marco del concurso “Alianzas Interinstitucionales para Programas de Doctorado”, según contrato PE501084299-2023-PROCIENCIA-BM.
REFERENCIAS
Aballay, F. H., Arriagada, G., Flores, G. E., & Centeno, N. D. (2013). An illustrated key to and diagnoses of the species of Histeridae (Coleoptera) associated with decaying carcasses in Argentina. ZooKeys, 261, 61–84. https://doi.org/10.3897/zookeys.261.4226
Aballay, F. H., Murúa, A. F., Acosta, J. C., & Centeno, N. D. (2012). Succession of carrion fauna in the arid region of San Juan province, Argentina: Its forensic relevance. Neotropical Entomology, 41, 27–31.
Arriagada, G., Jofré, F. N., & Aballay, F. H. (2019). Nueva especie de Euspilotus Lewis de Argentina (Coleoptera: Histeridae). Revista del Museo Argentino de Ciencias Naturales, 21(1), 7–15.
Bala, M., & Kaur, P. (2014). Insect faunal succession on buried piece of pork in the state of Punjab (India): A preliminary study. Journal of Forensic Research, 5, 252. https://doi. org/10.4172/2157-7145.1000252
Battán-Horenstein, M., Rosso, B., & García, M. D. (2012). Seasonal structure and dynamics of sarcosaprophagous fauna on pig carrion in a rural area of Cordoba (Argentina): Their importance in forensic science. Forensic Science International, 217(1–3), 146–156. https://doi.org/10.1016/j.forsciint.2011.10.043
Calzolari, M., Defilippo, F., Zani, G., Colombo, M., & Dottori, M. (2014). Characterization of necrophagus entomofauna in a typical agricultural area in Emilia-Romagna region (Northern Italy). Entomology, 2, 73–78.
Castillo-Miralbés, M. (2002). Estudio de la entomofauna asociada en el Alto Aragón (España). Monografías Sociedad Entomológica Aragonesa, 6, 1–94.
Caterino, M. S., & Tischechkin, A. K. (2015). Phylogeny and generic limits in New World Exosternini (Coleoptera: Histeridae: Histerinae). Systematic Entomology, 40, 109–110. https://doi.org/10.1111/syen.12095
Cobo, A., & Lancis, S. (1981). La putrefacción cadavérica al aire libre. Estudio médico-legal en las provincias de Santiago de Cuba, Granma y Guantánamo. Revista Actualidad de Medicina Legal, 1, 4–66.
Genaro, J. A., & Tejuca, A. E. (2001). Patterns of endemism and biogeography of Cuban insects. In: Woods, C. A. & Sergile, F. E. (eds.). Biogeography of the West Indies: Patterns and perspectives, 15–33. 2nd ed. CRC Press, 582 pp.
Gundlach, J. C. (1891). Contribución a la entomología cubana. Parte quinta: Coleópteros. Imp. de A. Alvarez y Comp, Riela núm. 40. La Habana, 71 pp.
Kovarik, P. W., & Caterino, M. S. (2000). Histeridae: 212–227. En Arnett, R. H., & Thomas, M.C. (Eds.). (2000). American Beetles, Volume I: Archostemata, Myxophaga, Adephaga, Polyphaga: Staphyliniformia (1st ed.). CRC Press. https://doi.org/10.1201/9781482274325
Lackner, T., Miles, Y. Z., Kindler, C., Motyka, M., & Balke, M. (2024). Saprininae: Phylogeny, biogeography and a new classification of the subfamily (Coleoptera: Histeridae). Systematic Entomology, 49(1), 48–71. https://doi.org/10.1111/syen.12606
Lamoth-Mayet, Y., & Posada, J. A. (2024). La Entomología Criminalística en Cuba: Proyecciones para su desarrollo. Revista Científica Multidisciplinar FARMHOUSE Ciencia & Tecnologia, 3(5), 10–13.
LeConte, J. E. (1860). Description of new species of the coleopterous family Histeridae. Proceedings of the Academy of Natural Sciences of Philadelphia, 11(1859), 310–317.
Lundyshev, D. S. (2017). New records of Atholus beetle species (Coleoptera, Histeridae) from Tanzania. Euroasian Entomological Journal, 16(1), 73–74.
Mariani, R., Mancuso, R. G., Varela, G. L., & Inda, A. M. (2014). Entomofauna of a buried body: Study of the exhumation of a human cadaver in Buenos Aires, Argentina. Forensic Science International, 237, 19–26.
Marseul, S. A. (1854). Essai monographique sur la famille des histérides (Suite). Annales de la Société Entomologique de France, (3) 1, 447–553.
Mazur, S. W. (1972). The Scientific Results of the Hungarian Soil Zoological Expeditions to South America, 22. The species of the family Histeridae (Coleoptera). Annales HistüricoNaturales Müsei Nation Alis Hungarici, 64, 184.
Megna, Y. S., Lamoth-Mayet, Y., Caterino, M. S., & Lackner, T. (2021). Phelister Marseul, 1854 in Cuba: first West Indies records of Phelister completus Schmidt, 1893, and notes on other Cuban species (Coleoptera, Histeridae, Histerinae). Check List, 17(1), 39–44. https://doi.org/10.15560/17.1.39
Mise, K. M., Correa, R. C., & Almeida, L. M. (2013). Coleoptera fauna found on fresh and frozen rabbit carcasses in Curitiba, Paraná, Brazil. Brazilian Journal of Biology, 73(3), 543–48. https://doi.org/10.1590/S1519-69842013000300012
Naranjo, C., Cruz, Y., & Mayea, Y. (2009). Artrópodos presentes en la putrefacción de cadáveres de cerdos (Sus scrofa) en Santiago de Cuba, Cuba. Boletín de la Sociedad Entomológica Aragonesa, 44, 441–447.
Paykull, G. (1811). Monographia Histeroidum. Upsaliae: Stenhammar & Pamblad, 114 pp.
Peck, S. B. (2005). A checklist of the beetles of Cuba with data on distribution and bionomics (Insecta: Coleoptera). Arthropods of Florida and neighboring land areas, 18, 123–125.
Peck, S. B., Ruiz-Baliú, A. E., & Garcés, G. G. (1998). The cave-inhabiting beetles of Cuba (Insecta: Coleoptera): diversity, distribution and ecology. Journal of Cave and Karst Studies, 60(3), 156–166.
Perez-Gelabert, D. E. (2020). Checklist, bibliography and quantitative data of the arthropods of Hispaniola. Zootaxa, 4749(1), 001–668. https://doi.org/10.11646/zootaxa.4749.1.1
Quensel, C. (1806). [New taxa]. En C. J. Schönherr (Ed.), Synonymia Insectorum, oder Versuch einer Synonymie aller bisher bekannten Insecten; nach Fabricii Systema Eleutheratorum geordnet, mit Berichtigungen und Anmerkungen wie auch Beschreibungen neuer Arten. Erster Band. Eleutherata oder Käfer. Erster Theil. Lethrus ... Scolytes. A. Nordström., xxii+ 293 pp.
Sagra, R. (1857). Historia física, política y natural de la isla de Cuba. Biblioteca digital Real Jardín Botánico (CSIC), 7, 44–49.
Santos, W. E., Alves, A. C., & Duarte, A. J. (2014). Beetles (Insecta, Coleoptera) associated with pig carcasses exposed in a Caatinga area, Northeastern Brazil. Brazilian Journal of Biology, 74(3), 49–55. https://doi.org/10.1590/bjb.2014.0072
Schmidt, J. (1893). Zwölf neue Phelister (Coleopt. Histeridae). Entomologische Nachrichten, 19, 8l–91.
Segura, N. A., Usaquén, W., Sánchez, M. C., Chuaire, L., & Bello, F. (2009). Succession pattern of cadaverous entomofauna in a semi-rural area of Bogotá, Colombia. Forensic Science International, 187(1–3), 66–72. https://doi.org/ 10.1016/j.forsciint.2009.02.018
Sokolov, A. V. (2005). Aditions to Hister beetles (Coleoptera: Histeridae) fauna of Cuba, with description of new species of genus Iliotona Carnochan, 1917. Russian Entomological Journal, 14(1), 83–85.
Sokolov, A. V. (2016). Description of a new species of Carcinops (Coleoptera: Histeridae) from Cuba. Russian Entomological Journal, 25(3), 237–238.
Yélamos, T. (2002). Fauna Ibérica. Coleoptera. Histeridae. Museo Nacional de Ciencias Naturales. Consejo Superior de Investigaciones Científicas, 17, 51.
Cómo citar: Lamoth-Mayet, Y., & Megna, Y. S. (2026). Grupos morfoecológicos de la familia Histeridae (Coleoptera: Polyphaga) de importancia criminalística en Cuba. Novitates Caribaea, (27), 1–17.
http://doi.org/10.33800/nc.vi27.386
ANEXO 1. MATERIAL EXAMINADO DE LAS ESPECIES DE HISTERIDAE DE CUBA
Hololepta (Hololepta) cubensis Erichson, 1834
Material examinado. CUBA: Pinar del Río, Finca, San Cristóbal, 01.vi.1958, I. García col., 1 (IZAC). Ciudad de la Habana, Santiago de las Vegas, 01.v.1930, I. García col., 1 (IZAC), 01.vii.1961, I. García col., 1 (IZAC), 15.viii.1961, I. García col., 2 (IZAC). Sancti Spíritus, Cafetal Gaviña. Escambray, 01.vii.1973, I. García col., 1 (IZAC). Camagüey, Loma La Llaga, Najasa, 01.v.1964, I. García col., 1 (IZAC).
Hololepta (Leionota) interrupta Marseul, 1853
Material examinado. CUBA: Ciudad de la Habana, Estación de experimentación agronómica, Santiago de las Vegas, 15.viii.1961, I. García col., 1 (IZAC).
Hololepta (Leionota) minuta Erichson, 1834
Material examinado. CUBA: Isla de la Juventud, La Victoria, 10.xii.1974, B. Zayas col., 1 (IZAC). Ciudad de la Habana, Estación de experimentación agronómica, Santiago de las Vegas, vi.1958, I. García col., 1 (IZAC).
Hololepta (Leionota) quadridentatum (Oliver, 1789)
Material examinado. CUBA: Pinar del Río, El Veral, Guanacabibes, xi.1965, I. García col., 1 (IZAC). Guantánamo, Cabo de San Antonio, 02.x.1963, Nicholes col., 1 (IZAC). Santiago de Cuba, Pico Turquino, 29.vi.1936, J. Acuña col., 1 (IZAC).
Euspilotus (Hesperosaprinus) cubaecola (Marseul, 1855)
Material examinado. CUBA: Santiago d e C u b a, Finca U n i v ersidad d e O riente, 1 4.iii.2010, 20.048°, -075.819°, Y. Lamoth col., 14 (CZCTR); II Frente, Mayarí, Cañada Amarilla, 09.ii.2019, Y. Lamoth col., 3 (CZCTR); Santiago de Cuba, Finca La Abundancia, 07.x.2011, Y. Lamoth col., 4 (CZCTR); El Cristo, Finca La Prudencia, 20.iii.2011, 20.110º, -75.733º, Y. Lamoth col., 2 (CZCTR); La Maya, Poblado Guaninicú. 15.iii.2011 Y. Lamoth col., 4 (CZCTR); Dos Palmas, Arroyo Grande, 17.vii.2010,Y. Lamoth col., 4 (CZCTR); El Cristo, Finca La Brujería, 16.iii.2011, Y. Lamoth col., 2 (CZCTR); Santiago de Cuba, Finca La Esperanza, Carretera de Siboney, 12.xii.2012, 19.989º, -75.723º, Y. Lamoth col., 1 (CZCTR); Santiago de Cuba, El Brujo, Carretera de Siboney, 15.v.2014, Y. Lamoth col., 2 (CZCTR); Santiago de Cuba, Finca Casa Azul, 06.iix.2011, 20.05º, -75.84º, Y. Lamoth col., 1 (CZCTR); Carretera Turística, km 4 ½. Reparto Altamira, 02.vii.2019, Y. Lamoth, col., 8 (CZCTR), Universidad de Oriente, 14.iii.2010; Y. Lamoth col., 15 (CZCTR), Carretera Central km 9 ½ Puerto Pelado, 29.v.2020, Y. Lamoth col., 2 (CZCTR); Carretera de Baconao, 17.vii.2020, Y. Lamoth col., 1 (CZCTR); Área protegida La Estrella-Aguadores, 01.ii.2021, Y. Lamoth col., 8 (CZCTR), Finca Bueno, Micro 7, Distrito José Martí, 23.ix.2021, Y. Lamoth col., 10 (CZCTR). Guantánamo, 20.iv.1914, 3 (CZCTR). Mayabeque, Nueva Paz, 12.iv.2010, I.
Jiménez col. 12 (IZAC); 22.iii.2010, I. Jiménez col., 5 (IZAC). Artemisa, Finca Roberto Negrín, 09 al 12.vii.2015, D. Sánchez, col., 14 (IZAC). La Habana, 10.v.1935, 10 (IZAC).
Euspilotus (Hesperosaprinus) arrogans (Marseul, 1855)
Material examinado. CUBA: Santiago de Cuba, Carretera de El Cobre, km 10, (03−04). ix.2018, 20, 064°, -75,843°, Y. Lamoth col., 6 (CZCTR); Carretera Turística, Fábrica de Cemento José Mercerón, 02.vii.2019, Y. Lamoth, col., 1 (CZCTR); Carretera de Baconao, Villa Daiquirí, 15.vi.2020, Y. Lamoth, col., 1 (CZCTR); Carretera del Aeropuerto, 02.vii.2019, Y. Lamoth, col., 8 (CZCTR). Mayabeque, N ueva Paz, 2 2.iii.2010, I. Jiménez, col., 2 (CZCTR).
Euspilotus (Hesperosaprinus) campechianus (Marseul, 1855)
Material examinado. CUBA: Santiago de Cuba, Santiago de Cuba, Carretera de El Cobre km 10, 02.ix.2018, Y. Lamoth col., 1 (CZCTR); Carretera Turística km 4 ½; Reparto Altamira, 02.vii.2019, Y. Lamoth, col., 1 (CZCTR). Guantánamo, 20.iv.1914, 1 (CZCTR).
Xerosaprinus fulgidus (LeConte, 1860)
Material examinado. CUBA: Santiago de Cuba, Carretera de El Cobre, km 10, 04.ix.2017, Y. Lamoth col., 1 (CZCTR).
Xerosaprinus viator (Marseul, 1855)
Material examinado. CUBA: Santiago de Cuba, Finca Universidad de Oriente, 1 4.iii.2010, Y. Lamoth col., 8 (CZCTR); Carretera Turística, km 4; Reparto Altamira, 02.vii.2019, Y. Lamoth, col., 4 (CZCTR), Carretera Central km 9 ½ Puerto Pelado, 26.v.2020, Y. Lamoth col., 28 (CZCTR); Carretera de Baconao km, 17.vii.2020, Y. Lamoth col., 69 (CZCTR); Carretera Central km 9 ½ Puerto Pelado, 23.vi.2020, Y. Lamoth col., 1 (IZAC); Carretera Central km 9 ½ Puerto Pelado, 02.vi.2021, Y. Lamoth col., 2 (IZAC); Área protegida La Estrella-Aguadores, 01.ii.2021, Y. Lamoth col., 18 (IZAC); Finca Bueno, Micro 7, Distrito José Martí, 22.ii.2021, Y. Lamoth col., 3 (IZAC); Camino Viejo del Cobre, km 8, La Sabana, 12.ix.2021, Y. Lamoth col., 3. Guantánamo, San Carlos, 03.v.1917, 10 (CZCTR).
Omalodes (Omalodes) laevigatus (Quensel, 1806)
Material examinado. CUBA: Santiago de Cuba, San Juan, 15.vi.2020, 6.934°-78.442°, Y. Lamoth col., 3 (CZCTR); Carretera Central km 9 ½ Puerto Pelado, 26.v.2020, Y. Lamoth col., 4 (CZCTR); Carretera de Baconao km, 19.vii.2020, Y. Lamoth col., 2 (IZAC); Carretera Central km 9 ½ Puerto Pelado, 24.vi.2020, Y. Lamoth col., 4 (IZAC); Carretera Central km 9 ½ Puerto Pelado, 20.ii.2021, Y. Lamoth col., 1 (CZCTR); Finca Bueno, Micro7, Distrito José Martí, 23ix.2021, Y. Lamoth col., 1 (IZAC). Guantánamo, col., 2 (CZCTR).
Omalodes (Omalodes) ruficlavis Marseul, 1853
Material examinado. CUBA: Guantánamo, San Carlos, 03-v-1917, 10 (CZCTR).
Hister coenosus Erichson, 1834
Material examinado. CUBA. Santiago de Cuba, Finca Universidad de Oriente, km 10, 14.iii.2017, Y. Lamoth col., 7 (CZCTR); Finca La Abundancia, 07.x.2011, Y. Lamoth col., 5 (CZCTR); El Cristo, Finca La Prudencia, 20.iii.2011, Y. Lamoth col., 3 (CZCTR); La Maya, Poblado Guaninicú.15.iii.2011, Y. Lamoth col., 1 (CZCTR); Dos Palmas, Arroyo
Grande, 17.vii.2010, Y. Lamoth col., 1 (CZCTR); Carretera Central km 9 ½ Puerto Pelado, 22.vi.2021, Y. Lamoth col., 3 (CZCTR); San Juan, 4030 m, 9.vi.2020, 6.934°, -78.442°,
Y. S. Megna col., 3 (CZCTR); San Juan, 13.vi.2020, 6.934°, -78.442°, Y. Lamoth y Y. S. Megna col., 12 (CZCTR); San Juan, 15.vi.2020, 6.934°, -78.442°, Y. Lamoth col., 3 (CZCTR); Carretera de Baconao, 17.vii.2020, Y. Lamoth col., 2 (CZCTR); Camino al Matadero, 24.ix.2021, Y. Lamoth col., 7 (IZAC); Área protegida La Estrella-Aguadores, 01.ii.2021, Y. Lamoth col., 1(IZAC); Camino Viejo del Cobre, km 8, La Sabana, 12.ix.2021, Y. Lamoth col., 1. Guantánamo, 20.iv.1917, 3 (CZCTR). Mayabeque, Nueva Paz, 12.iv.2010, I. Jiménez col., 4; 22.iii.2010, I. Jiménez col., 2 (IZAC). Holguín, 7 km al Sur de la Villa Guardalavaca, 20.x.2003, 3 (CZCTR). Granma, Dos Ríos, Jiguaní, Próximo al río Contramaestre, 29.xii.2020, Y. Lamoth col., 1 (IZAC).
Phelister haemorrhous Marseul, 1854
Material examinado. CUBA: Santiago d e C uba, Finca U n i v ersidad de O riente, 1 4.iii.2010, Y. Lamoth col., 2 (CZCTR); Carretera de El Cobre, km 10, 25.ii.2017, Y. Lamoth col., 2 (CZCTR); Universidad de Oriente, 16.xi.1947, 3 (CZCTR); Vista Alegre, 14.iii.2010, 2 (CZCTR); San Juan, 4030 m, 9.vi.2020, 6.934°, -78.442°, Y. S. Megna col., 6 (CZCTR); San Juan, 13.vi.2020, 6.934°, -78.442°, Y. Lamoth y Y. S. Megna col., 18 (CZCTR); San Juan, 15.vi.2020, 6.934°, -78.442°, Y. Lamoth col., 46 (IZAC); Carretera de Mar Verde km 7, 22.vi.2021, Y. Lamoth col., 3 (IZAC); Carretera de Mar Verde km 10, 19.vi.2021, Y. Lamoth col., 2 (IZAC); Camino al Matadero, 24.ix.2021, Y. Lamoth col., 2 (IZAC); Carretera Central km 9 ½ Puerto Pelado, 23.vi.2020, Y. Lamoth col., 1(IZAC). Granma, Dos Ríos, Jiguaní, Próximo al río Contramaestre, 29.xii.2020, Y. Lamoth col., 1 (IZAC).
Phelister completus Schmidt, 1893
Material examinado. CUBA: Santiago de Cuba, Cuabitas, 14.iii.2010, Y. Lamoth col., 1 (CZCTR).
Phelister panamensis LeConte, 1859
Material examinado. CUBA: Santiago de Cuba, Carretera de El Cobre, km10, 24-27.ii.2017, Y. Lamoth col., 8 (CZCTR); San Juan, 13.vi.2020, 6.934°, -78.442°, Y. Lamoth y Y. S. Megna col., 36 (CZCTR); San Juan, 15.vi.2020, 6.934°, -78.442°, Y. Lamoth col., 38 (CZCTR); Carretera de Baconao, 17.vii.2020, Y. Lamoth col., 15 (CZCTR); Carretera de Mar Verde km 7, 23-vi-2021, Y. Lamoth col., 1 (CZCTR); Camino al Matadero, 24.ix.2021, Y. Lamoth col., 2 (CZCTR); Carretera Central km 9 ½ Puerto Pelado, 23.vi.2020, Y. Lamoth col., 5 (CZCTR); Carretera Central km 9 ½ Puerto Pelado, 22.ii.2021, Y. Lamoth col., 1 (CZCTR); Área protegida La Estrella-Aguadores, 01-ii-2021, Y. Lamoth col., 1 (IZAC); Finca Bueno, Micro7, Distrito José Martí, 23.ix.2021, Y. Lamoth col., 3 (IZAC). Granma, Dos Ríos, Jiguaní, Próximo al río Contramaestre, 29.xii.2020, Y. Lamoth col., 1 (IZAC). Artemisa, Sierra de Anafe, 23.xi.1934, 2 (IZAC).
Atholus confinis (Erichson, 1834)
Material examinado. CUBA: Santiago de Cuba, Carretera de El Cobre, km 10, 24-26. ii.2017, Y. Lamoth col., 6 (IZAC); Camino al matadero, Carretera del Cobre, 26.ix.2021, Y. Lamoth col., 1(CZCTR); Carretera de Mar Verde km 7, 22.vi.2021, Y. Lamoth col., 3 (CZCTR). Guantánamo, col., 1 (CZCTR).
Carcinops troglodytes (Paykull, 1811)
Material examinado. CUBA: Santiago de Cuba, Carretera de Mar Verde km 7, 22.vi.2021, Y. Lamoth col., 3 (CZCTR).
Epierus antillarum (Marseul, 1854)
Material examinado. CUBA: La Habana, Finca Coca, San Antonio de los Baños, v.1961, I. García col., 4 (IZAC). Guantánamo, Cueva La Patana, 3 (CZCTR). Holguín, Cueva de las Cuatrocientas Rozas, 2 (CZCTR). Santiago de Cuba, Finca Bueno, Micro 7, Distrito José Martí, 31.v.2021, Y. Lamoth col., 6 (CZCTR); Finca Bueno, Micro 7, Distrito José Martí, 23.ii.2021, Y. Lamoth col., 4 (CZCTR).
Acritus ignobilis Lewis, 1888
Material examinado. Santiago de Cuba, Finca Bueno, Micro 7, Distrito José Martí, 23.ix.2021, Y. Lamoth col., 10 (CZCTR).